| 会议详情 |
|

推荐会议:2026药未来峰会
发票类型:增值税普通发票 增值税专用发票
南京传奇生物科技有限公司
大会背景
药品是生命安全的保障,因其特殊性,药品质量的管控更是重中之重。国内打出“质量”口号的药企不在少数,但到关键时刻,质量往往被居于次要地位。
近两年,随着国家药监政策的不断出台,“四个最严”和飞行检查的常态化,严把质量关已是大势所趋,药企质量部门需要更多高素质人员负责监管药品质量,且一致性评价及药品研发同样需要将质量延伸到药品生命周期的研发前端,真正实现“质量源于设计”的理念。
大分子生物药由于其结构复杂、质控难度大,随着技术的发展,检测方法的不同、仪器的更新,无疑在促使我们需要更加深层次的了解分析及药物研究。
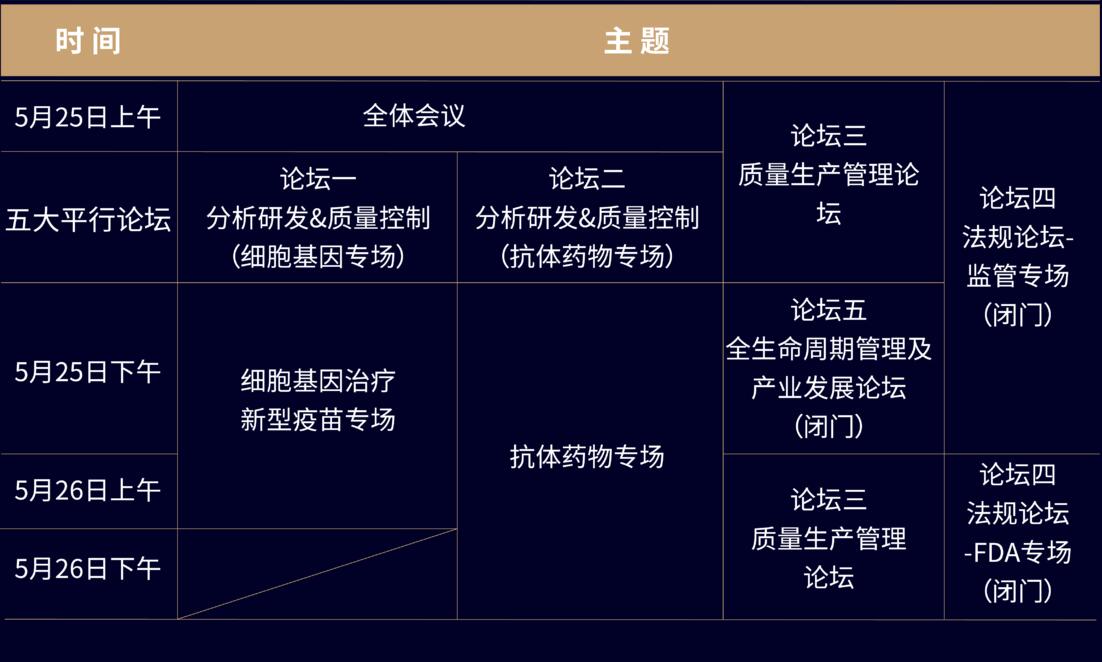
基于此,2021年QbD第二届生物药质量科学大会特设五大平行专场论坛,召集1000+行业专家、50+权威大咖与会,共同探索研讨,助力国内企业药品质量提升、质量管理体系健全,与国际规范并轨。
QbD第二届生物药质量科学大会信息
大会主题 | 将质量理念融入分析研发与生产管理
主办单位 | 佰傲谷-生物医药领先聚合社区
协办单位 | 中国医药设备工程协会、DataRevive USA LLC
大会时间 | 2021年5月25日-26日
大会地点 | 北京·朗丽兹西山花园酒店
大会规模 | 800-1000人
合作媒体 | 生物制药小编、药渡、新药创始人俱乐部、药学进展、制药在线、肽度、医药合作投融资联盟、药融圈、药通社、药物一致性评价、药物分析之家、药物简讯,生物探索等40家顶尖媒体助阵报道。
大会亮点
10+生物药质量大拿联合策划
国内第一个聚焦生物药质量领域的千人分析科学大会
五大论坛+短培训+卫星会+直播
深度和广度并存,全方面满足参会者不同需求
从监管考量到企业实践
抽丝剥茧,探索不同新政背后的合规要求
从分析研发到生产质量管理,深耕QC、QA体系标准
做到生物医药质量方向的全产业链内容
监管机构、生物制药行业上下游企业同聚一堂
共同探讨产业发展中的问题,促进行业不断进步
参会群体
Bio-Tech/Pharm
※质量部QA/QC部※研发部、制剂部、注册部※工艺开发部※技术部、生产部※医学事务部※项目管理及公司高管相关人员
院校/监管机构
※科研人员※法规专家※注册申报※审查人员
第三方技术服务咨询公司
※CRO、CDMO※法规咨询、质量检测服务从业人员等

热点议题
全体大会
1新形势·新阶段·新思考-全球生物新药质量监管趋势分析与应对
2药明生物-中国最大的CDMO是如何管理质量的?
3从药品检验技术的应用看我国药品质量控制的发展
4制药行业质量检测发展趋势
5做国际化创新药在质量和生产方面的挑战与策略
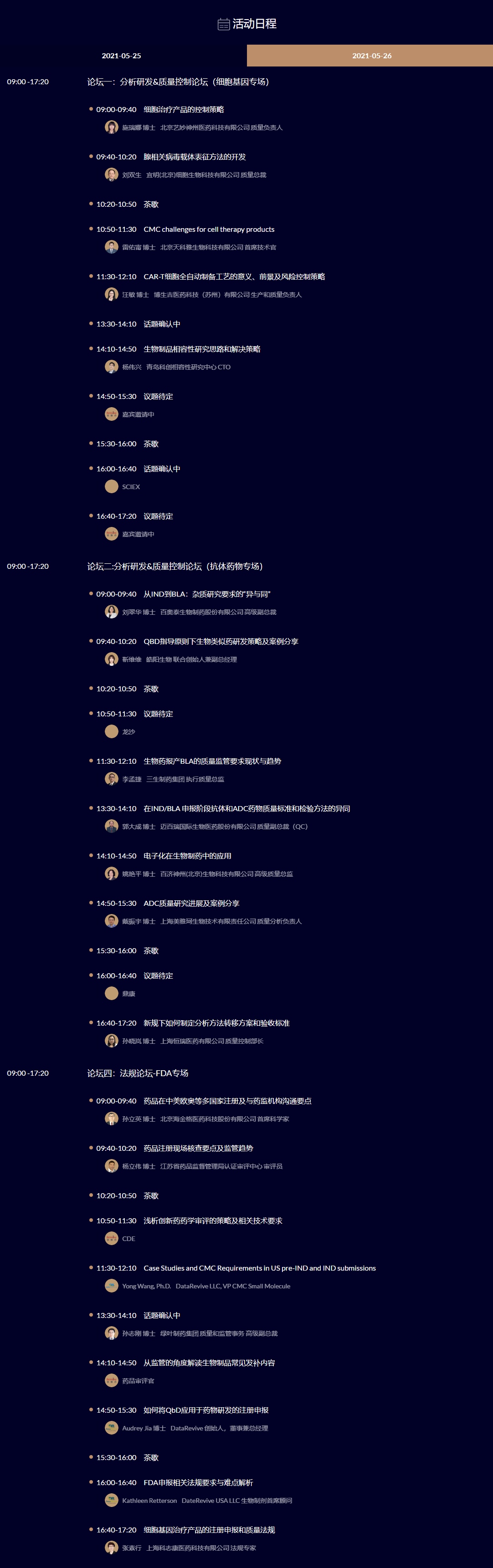
分析研发&质量控制论坛(抗体药物专场)
1生物制品研发质量管理体系的建立-从细胞株到产品上市
2在IND/BLA申报阶段抗体和ADC药物质量标准和检验方法的异同
3氢/气交换质谱法表征复杂结构抗体类药物的应用
4新规下如何制定分析方法转移方案和验收标准
5从IND到BLA:杂质研究要求的“异与同”
6ADC电荷异质性分析(暂拟)
7双特异性抗体的质量研究和杂质控制策略
8聚体表征的研究进展及案例分析
分析研发&质量控制论坛(细胞基因&新型疫苗专场)
1CAR-T细胞质量控制方法及注册检验相关问题
2细胞基因产品成药性思考和可开发性评估
3流式在质控方面的应用
4合规的QC实验室管理运营模式
5细胞治疗产品质量标准制定的关键要点
6基因治疗药物质量控制研究的最新要求解析
7疫苗质量控制和质量标准的建立
8CAR-T制品中残留物的分析策略
9如何实现细胞制剂产品放行检快检
质量法规论坛-监管专场(5月25日)
1生物制剂的监管/生物制品GMP附录
2生物制品药典附录解读
3疫苗保供
4《生物安全法》的相关解读及对产业的影响
5关于市场或供应链安全:全球疫苗供应体系
6生物药品的注册核查新要求/程序
7ICH-Q5E指南总结与分析
质量法规论坛-FDA专场(5月26日)
1药品在中美欧奥等多国家注册及与药监机构沟通要点
2细胞基因治疗产品IND/BLA评审要点
3从监管的角度解读生物制品常见发补内容
4浅析创新药药学审评的策略及相关技术要求
5中美申报上市药品风险评估和应对的思考
6如何将QbD应用于药物研发的注册申报
7ICHQ6B生物技术/生物产品的检验程序和可接收标准研读
8FDA申报相关法规要求与难点解析
生产与质量管理论坛
1ICH Q13与连续化制造
2ADC商品化生产质量关注点
3《生物制品MAH的全生命周期质量管理》
4实时放行PAT技术
5生物药原液不锈钢设施的设计、建设和验证
6在满足监管的条件下实现抗体药物的工艺改进与工艺变更的关键考虑
7生物制药的连续化制造
8单抗药物生产设施暖通设计要点探讨
更多热点议题及大会议程陆续更新中......
已确认嘉宾
* Michele Dougherty前FDACMC审评主任 DataRevive副总裁
*陶铜静复星凯特质量负责人
*郑杰中国科学院上海药物研究所研究员
*施立明创胜集团分析科学及质量控制副总裁
*刘翠华百奥泰高级副总裁
*曹艳华南京驯鹿医疗技术有限公司质量总监
*孙立英北京海金格首席科学家、前FDA审评组长
*张素行上海科志康法规专家
*郭大成迈百瑞质量副总裁
*Audrey Jia DataRevive创始人、董事兼总经理、前FDA审评官
*Kathleen Retterson DataRevive生物制剂首席顾问
*李壮林荣昌生物副总裁
*许建辰诺和诺德质量副总监
*臧恒昌山东大学药学院教授
* Michael Garvey百济神州副总裁
*周新华嘉和生物药业有限公司总裁
*李树德天境生物副总裁
*姚艳平百济神州(北京)生物科技有限公司高级质量总监
*孙志刚绿叶制药集团质量和监管事务高级副总裁
*李孟捷三生制药集团执行质量总监
*蒋彩花上海复宏汉霖生物制药有限公司质量高级副总裁
*施瑞纳北京艺妙神州医药科技有限公司高级质量总监
*孙晓岚恒瑞质量控制部长
*刘双生宜明(北京)细胞生物科技有限公司质量总裁
拟邀嘉宾
*黄岗药明生物高级副总裁
*郭中平国家药典委员会生物制品标准处处长
*王董明信达生物高级副总裁
*张萍基石药业质量管理VP
*马勇斌贝达药业副总裁
*朱祥平天境生物分析开发部负责人
*张鹏康方生物高级副总裁
*王亚君药明巨诺质量负责人
*马卫东康宁杰瑞质量副总裁
*饶春明中检院生检所主任
*刘革上海泽润生物副总裁
*王阳神州细胞副总经理
*吉申齐辉瑞中国区药品注册文件出版中心负责人
退票说明:不支持退票
报名成功后,不接受任何形式的退票行为。
报名成功后,如需发票,请在报名时做好登记,将在会后开具电子发票至个人报名邮箱。
 北京朗丽兹西山花园酒店
北京朗丽兹西山花园酒店
交通指南:
上地产业园、西三旗 驾车距离8.5公里(约18分钟); 南苑机场 驾车距离38.6公里(约97分钟); 首都国际机场 驾车距离38.0公里(约112分钟); 北京西站 驾车距离22.8公里(约73分钟)
北京朗丽兹西山花园酒店位于北京海淀北部核心商务区,紧邻永丰及中关村四大高科技园区;著名旅游区颐和园、圆明园、大觉寺皆近在咫尺,西山美景与您相伴。
这是一家集温泉、会议、商务、休闲及度假于一体的度假型会议酒店,占地面积约12万平米,拥有800余间(套)典雅、舒适的客房,豪华富矿温泉;雍容华贵的大型宴会厅总面积6000余平米;私密优雅地阳光餐厅、设施完善的休闲娱乐项目。
酒店全面覆盖美国RGF空气净化系统,并收藏了齐白石老先生的真迹及其弟子的真迹画作百余幅,经典与现代在这里完美结合,喧嚣都市中营造一片心灵的净土,是您休闲度假及商务会议的首选之地。
相关会议
2026-04-17上海