| 会议详情 |
|

推荐会议:CMIS 2026第七届中国医药数智峰会
发票类型:增值税普通发票 增值税专用发票
 BMAP
BMAP
在当今快速变化的商业环境下,BMAP主要致力于为生命科学行业领先的专业人士提供无与伦比的专业知识,最新的资讯和世界级的专业服务来促进业务的增长。 在BMAP举办的活动中,我们通过广泛的专业调研,以创新的形式,聚集生命科学行业的领先实践者和专家学者,探讨最前沿的信息知识,以帮助行业专业人士应对当今不断升级的挑战。作为领先的信息服务提供商,BMAP提供丰富的内容来帮助业内企业提高质量标准,保证安全,不断创新和降低风险,以适应日益规范的市场环境。
近些年来,整个医药行业大力追捧前途似锦的生物制药,传统的化学药市场似乎受到了冷落。生物制药的各类新闻,会议占据着各媒体的头版头条,仿佛我国的化学药 领域已经非常成熟。然而事实是我国的化药市场仍然面临全方位的技术挑战,同时许多创新型企业仍然专注于化学小分子新药的研制。
又恰逢今年药品相关的新法规及政策频出,新药品上市许可人制度,新版药典,临床实验自查,包材相容性,仿制药一致性评价等重磅新政让药企应接不暇,行业面临洗牌压力。如何更好地理解,并与监管机构交流政策,以及如何实施,是药企目前目前面临的最大挑战之一。
在此背景下,中国国际化学制药研究与开发论坛作为行业内的年度品牌峰会,将会聚集国内药品监管机构官员,行业意见领袖,国内领先化学制药企业以及全球大药厂代表,就最新的化学药品注册法规变化、仿制药一致性评价、新靶点发现、化合物开发与筛选策略,剂型创新与给药途径改良,以及临床前、临床模型设立等系列等 热点话题进行剖析,并提供高实践性的解决方法和思路,使企业更加合规、高效、低成本地开发化学药物。
活动亮点
提供了与国内外领先行业领袖以及专家交流的平台
了解最新国内外法规变化以及未来趋势,确保产品合规
获悉市场和法规新动态,从而制定最佳研发战略
理解技术要点并确保化学仿制药的一致性
探索化药中创新突破的多种机遇与可能
通过案例研究和讨论,领略前言药品研发成果
WCPF旨在帮助中国化学医药企业:
与中国和世界各国的领先行业领袖和行业专家学者建立关系
了解最新的中国及国际法规变化和未来趋势,确保产品合规
获知最新的市场和法规情报,以制定研发的最佳战略
理解技术要点并确保化学仿制药的一致性
探索化药中创新突破的多种机遇与可能
通过实际的案例研究和讨论,领略最前沿的药品研发成果
精彩议题:
近期法规热点解析
新药品上市许可人制度,会给中国企业带来怎样的冲击或调整?
新《药品注册管理办法》,药品注册管理等方面的调整,与企业发展息息相关。
新版cGMP实践有困难?请听领先企业来分享宝贵经验。
仿制药分论坛:确保与原研药的一致性
一致性评价标准与申报精准解读,不容错过。
如何确保数据的完整性、真实性、溯源性?
反向工程是仿制药研发的必经之路,如何利用反向工程提高仿制药品质?
创新药分论坛:高效、低成本地开发化学新药
如何探索一种安全、绿色、高效和稳定的原料药生产工艺?
改良剂型或者改变给药途径如何提升药效?
进一步加强研发与临床合作,转化医学对新药研发有重大推动作用。
WCPF旨在帮助中国化学医药企业:
与中国和世界各国的领先行业领袖和行业专家学者建立关系
了解最新的中国及国际法规变化和未来趋势,确保产品合规
获知最新的市场和法规情报,以制定研发的最佳战略
理解技术要点并确保化学仿制药的一致性
探索化药中创新突破的多种机遇与可能
通过实际的案例研究和讨论,领略最前沿的药品研发成果
主要参会群体:
领先化药公司的业务拓展部、产品开发部、研发部、 技术部、质量部,注册部的高级管理人员
杰出研究机构以及各大院校的科学家
药品审评机构的官员
中小型化药公司的企业家
CRO以及CMO的高级管理人员
化药科研,生产,质控等解决方案供应商
信息服务提供商的高级管理

|
2016年11月10日 星期四 北京金茂万丽酒店 |
||
|
时间 |
演讲题目 |
演讲嘉宾 |
|
08:50-09:00 |
欢迎致辞 |
|
|
近期法规热点解析 |
||
|
09:00-09:45 |
新药品上市许可人制度对中国医药研发影响的解读 |
杨悦 沈阳药科大学教授; 国家食品药品监督管理局高级研修学院客座教授 |
|
09:45-10:30 |
新版药典变化解读及与欧美药典的比较 |
钱忠直 国家药典委员会首席专家 |
|
10:30-11:00 |
茶歇 |
|
|
11:00-11:45 |
临床实验自查关键点剖析 |
张震 前药品评审中心专家 邀请中 |
|
11:45-12:25 |
国内外热点化学药品种和热点疾病领域分析 |
严尚军 艾美仕市场调研咨询(上海)有限公司咨询总监 |
|
12:30-14:00 |
午餐 |
|
|
领先企业实践案例分享 |
||
|
14:00-14:45 |
药企投资并购案例分享 |
刘学军 上海复星医药研究院副院长 |
|
14:45-15:15 |
eCTD电子申报 |
天津爱思爱科技有限公司 |
|
15:15-15:45 |
茶歇 |
|
|
15:45-16:30 |
专题讨论:中国药品申报美国/欧洲主要挑战和成功案例分享 |
主持:赵大川 华海/美国普霖斯通制药公司执行总监;普霖贝利生物制药公司高级副总经理 讨论嘉宾: 习宁 广东东阳光药业首席科学官 陈洪 以岭研究院药物研发副院长 |
|
16:30-17:15 |
高层圆桌讨论:企业研发战略思考与思路,以应对日益严格的法规环境 |
主持: 杜冠华 中国医学科学院药物研究所副所长 邀请中 讨论嘉宾: 吴飚 中国医药质量管理协会副会长 郞志慧 拜耳处方药事业部中国副总裁及医学 部总监 夏明德 美国强生集团亚太创新中心资深总监 吴振平 和记黄埔医药资深副总裁 |
|
17:50 |
会议结束 |
|
|
2016年11月11日 星期五 北京金茂万丽酒店 |
||
|
仿制药分论坛:确保与原研药的一致性 |
||
|
时间 |
演讲题目 |
演讲嘉宾 |
|
一致性评价 |
||
|
09:00-09:45 |
一致性评价审核方评价标准和申报程序解读 |
许鸣镝 中国食品药品检定研究院化药所副所长 邀请中 |
|
09:45-10:30 |
溶出曲线测定的方方面面 |
余立 北京市药品检验所所长助理; 国家食品药品监督管理局和北京市药品审评专家 |
|
10:30-11:00 |
茶歇 |
|
|
11:00-11:45 |
辅料与包材的质量控制与一致性评价 |
孙会敏 中国食品药品检定研究院包装材料与药用辅料检定所所长 |
|
11:45-12:15 |
从临床基地出发-成功达成一致性评价的生体等效性试验策略 |
曾宣凯 徐医佳生医药科技(徐州)有限公司临床研究发展处总监 |
|
12:30-14:00 |
午餐 |
|
|
14:00-14:45 |
基于杂质谱的仿制药质量一致性评价研究进展 |
张启明 中国食品药品检定研究院专家 |
|
14:45-15:30 |
如何确保数据完整性及数据完整性证明产品一致性问题分析 |
TBD |
|
15:30-16:00 |
茶歇 |
|
|
仿制药中的晶型/手性研究 |
||
|
16:00-16:45 |
晶型在化学药开发中的重要角色 |
陈敏华 苏州晶云药物科技有限公司首席执行官 |
|
仿制药的反向工程研究 |
||
|
16:45-17:30 |
如何利用反向工程提高仿制药品质 |
陈洪 以岭研究院药物研发副院长 |
|
2016年11月11日 星期五 北京金茂万丽酒店 |
||
|
创新药分论坛:高效、低成本地开发化学新药 |
||
|
时间 |
演讲题目 |
演讲嘉宾 |
|
化合物创新 |
||
|
09:00-09:45 |
更加高效、低成本的化合物发现和筛选策略 |
TBD |
|
09:45-10:30 |
探索一种安全、绿色、高效和稳定的原料药生产工艺 |
杜争鸣 百济神州高级副总裁,药学部首席总监 |
|
10:30-11:00 |
茶歇 |
|
|
创新剂型/给药途径改变与药效 |
||
|
11:00-11:45 |
早期制剂研发注意事项 |
陆明秋 罗氏研发(中国)制剂部负责人 |
|
11:45-12:30 |
长效GLP-1和口服给药最新进展 |
胡邵京 浙江贝达药业副总兼首席化学家 |
|
12:30-14:00 |
午餐 |
|
|
14:00-14:45 |
长效靶向制剂的研发思路分享 |
李又欣 绿叶制药集团高级副总裁、研发负责人 |
|
临床前/临床研究 |
||
|
14:45-15:30 |
量身定制的新药早期研发策略 |
黄悦 默克雪兰诺全球早期发展部中国临床药理部负责人 |
|
15:30-16:00 |
茶歇 |
|
|
16:00-16:45 |
临床试验模型案例分享 |
申华琼 强生制药有限公司中国临床研发总负责人 |
|
工艺优化与质量控制 |
||
|
16:45-17:30 |
制剂工艺研究与产品开发中技术关键点 |
TBD |
|
17:30-18:15 |
原料药物工艺优化与质量控制 |
杨劲松 勃林格殷格翰CoC化学中心负责人 邀请中 |
.jpg!hdj123)
杨劲松
勃林格殷格翰
CoC化学中心负责人
.jpg!hdj123)
申华琼
强生医药
副总裁
.jpg!hdj123)
黄悦
默克雪兰诺有限公司
中国临床药理部负责人
.jpg!hdj123)
李又欣
绿叶制药集团
研发副总裁
.jpg!hdj123)
胡邵京
浙江贝达药业股份有限公司
副总兼首席化学家
.jpg!hdj123)
陆明秋
罗氏研发(中国)有限公司
制剂部主任
.jpg!hdj123)
杜争鸣
百济神州(苏州)生物科技有限公司
高级副总裁
.jpg!hdj123)
陈敏华
苏州晶云药物科技有限公司
首席执行官
.jpg!hdj123)
张启明
中国食品药品检定研究院
专家
.jpg!hdj123)
曾宣凯
徐医佳生医药科技(徐州)有限公司
临床研究发展处总监
.jpg!hdj123)
孙会敏
中检院包装材料与药用辅料检定所研究员
所长
.jpg!hdj123)
余立
北京市药品检验所
所长助理
.jpg!hdj123)
吴振平
和记黄埔医药
资深副总裁
.jpg!hdj123)
夏明德
美国强生集团
资深总监
.jpg!hdj123)
郞志慧
拜耳处方药事业部
中国副总裁及医学部总监
.jpg!hdj123)
吴飚
中国医药质量管理协会
副会长
.jpg!hdj123)
陈洪
以岭研究院
药物研发副院长
.jpg!hdj123)
习宁
广东东阳光药业
首席科学官
.jpg!hdj123)
赵大川
普霖贝利生物制药
高级副总经理
.jpg!hdj123)
刘学军
上海复星医药研究院
副院长
.jpg!hdj123)
严尚军
艾美仕市场调研咨询(上海)有限公司
咨询总监
.jpg!hdj123)
钱忠直
国家药典委员会
首席专家
.jpg!hdj123)
杨悦
沈阳药科大学
教授
 北京金茂万丽酒店
北京金茂万丽酒店
北京金茂万丽酒店地处北京市中心——王府井大街,临近天安门广场和北京人民艺术剧院,周围热闹非凡,一直以来都是购物、旅游的中心。 北京金茂万丽酒店每间客房都融汇了现代科技与温馨典雅的色调,其中西区客房可欣赏到紫禁城的美景。 宾客可以方便地前往附近的小吃街享用当地美食,也可以在酒店的餐厅和酒吧品尝时尚美食佳肴。 近1000平米的宴会厅在王府井地区位列前茅,并设有五间可灵活布置的会议室,可满足您会议和宴会的需求。酒店设施时尚现代,设有室内泳池、先进的健身中心和水疗中心,为宾客悉心打造健康生活方式,让宾客在繁华地段尽享商旅体验。 交通:机场大巴王府井金宝街线---王府井大街(天伦王朝酒店)站 下车---步行 370米
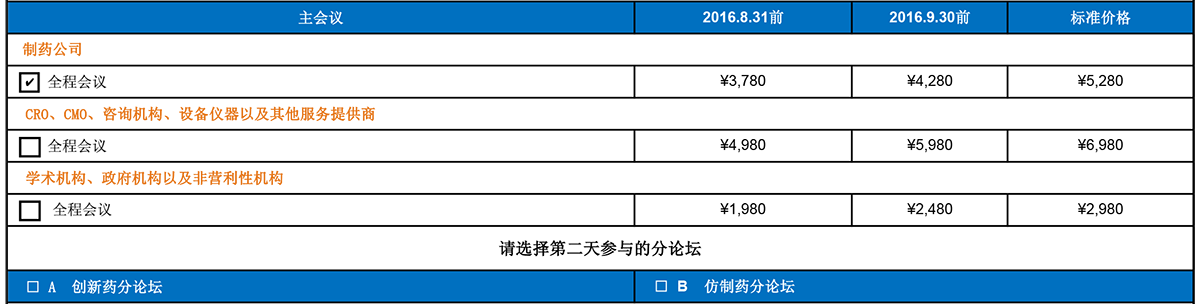
以上的优惠价格体系在截止日期内有效。所有的费用都需要在规定的有效日期内付款,否则将自动跳到下一个价格水平层。
制药企业管理人员的价格:若申请此价格,贵公司必须研发并生产医药产品。BMAP对此价格保留审合的权利。
订单条款
付款原则
需要在收到发票后的10天内全额付款以确认注册成功,否则席位将有可能被取消掉。
所有的付款必须在会议开展前完成。您所缴纳的费用包括大会的入场券、茶歇、午餐、会议手册以及根据政府规定的相应税金。
请注意住宿以及交通费用不包括在上述价格内。价格与折扣原则
为了保障您的优惠价格席位,请您在优惠截止日期前提交注册表格并完成付款。
如果在您收到发票后的10天之内未完成付款,优惠价格将不再保留并自动生成为当期价格。
如果同一组织机构有3位或3位以上的工作人员参加可享受当期价格9折优惠,请注意团队优惠价格只提供给3人以上团队同时注册并由同一组织机构付款。取消与替代原则
一旦确认注册成功就不能取消,但是如果您无法参加,欢迎推荐替代参会者。请在第一时间提交替代参会者信息。
不管BMAP以任何理由取消此次活动,您所交付的款项将全额退还。
不管BMAP因为何种客观原因将活动延迟而致使参会人员无法如期参加的话,参会人员都将得到有BMAP提供的全额保值单据。您可以使用此单据参加任何一年内同等价值的活动。
除了以上的情况,任何其他形式的取消都将不会提供保值单据。
对于任何活动的改期、延迟和取消,BMAP无法对因为替代参会人员而产生的损失负责。如因不可抗拒的自然灾害、不可预见的突发事件或者任何其它客观原因导 致此次活动无法进行,BMAP对此不负任何法律责任。此条款中陈述的不可预见的突发事件包括但不仅仅限于:战争、火灾、罢工、极端天气或其他类似情况。
相关会议
2026-03-28上海
2026-03-26成都